Mirtazapin
- Seiten mit Skriptfehlern
- Wikipedia:Vorlagenfehler/Vorlage:EDQM
- Wikipedia:Vorlagenfehler/Vorlage:Sigma-Aldrich
- Wikipedia:Vorlagenfehler/Vorlage:Cite journal/temporär
- Wikipedia:Vorlagenfehler/Vorlage:Cite journal
- Wikipedia:Vorlagenfehler/Vorlage:Infobox Chemikalie
- Wikipedia:Wikidata-Wartung:PubChem abweichend
- Wikipedia:Wikidata-Wartung:DrugBank abweichend
- ATC-N06
- Wikipedia:Wikidata-Wartung:CAS-Nummer fehlt lokal
- Pyridin
- Dihydroazepin
- Piperazin
- Aromat
- Antidepressivum
- Arzneistoff
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
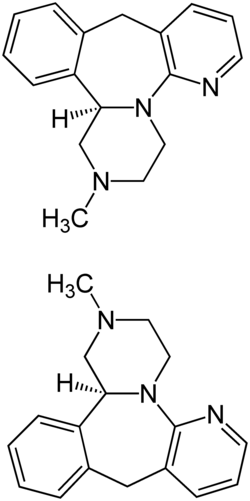
| |||||||||||||
| (R)-Enantiomer (oben) und (S)-Enantiomer (unten) | |||||||||||||
| Allgemeines | |||||||||||||
| Freiname | Mirtazapin | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C17H19N3 | ||||||||||||
| Kurzbeschreibung |
weißes oder fast weißes, leicht hygroskopisches Pulver[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Arzneistoffangaben | |||||||||||||
| ATC-Code | |||||||||||||
| Wirkstoffklasse |
Antidepressivum | ||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 265,35 g·mol−1 | ||||||||||||
| Schmelzpunkt |
114–116 °C [(RS)-Mirtazapin][2] | ||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser, leicht löslich in absolutem Ethanol[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Mirtazapin ist das Pyridyl-Analogon von Mianserin und ein Arzneistoff aus der Gruppe der tetrazyklischen Antidepressiva. Mirtazapin wurde 1976 erstmals patentiert[2].
Pharmakologie
Mirtazapin gilt als ein noradrenerg und spezifisch serotonerg wirkendes Antidepressivum (NaSSA): Es besetzt im Gehirn verschiedene Bindungsstellen für Botenstoffe und verändert damit den Einfluss dieser Botenstoffe auf den Gehirnstoffwechsel. Insbesondere steigert es die Freisetzung von Noradrenalin und Serotonin und erhöht so deren Wirkung. Neuere Untersuchungen haben allerdings ergeben, dass die serotonerge Wirkung nur sehr schwach ausgeprägt ist.[4]
Wirkprinzip (Pharmakodynamik)
Mirtazapin bewirkt eine Blockade zentraler präsynaptischer α2-Rezeptoren und dadurch eine Hemmung verschiedener Koppelungs- und negativer Feedbackmechanismen, über die normalerweise die Freisetzung der Neurotransmitter Serotonin und Noradrenalin gehemmt wird. Laut Hersteller tritt als Folge eine verstärkte Freisetzung von Serotonin und Noradrenalin auf.[5] Eine relevante Verstärkung der Serotoninfreisetzung konnte jedoch in Studien und Tierversuchen nicht bestätigt werden.[4][6] Vielmehr konnte in Tierversuchen hauptsächlich eine Steigerung der Noradrenalin- und Dopaminfreisetzung beobachtet werden.[6] Die Substanz hemmt ferner die Serotoninrezeptoren vom Typ 5-HT2 und 5-HT3, nicht jedoch jene vom Typ 5-HT1, wodurch die Serotoninwirkung auf den 5-HT1-Rezeptortyp relativ verstärkt wird; dies ist für die Bezeichnung spezifisch serotonerg verantwortlich. Letztlich sorgt die ausgeprägte Hemmwirkung auf den H1-Rezeptor für die stark sedierenden Eigenschaften von Mirtazapin. [6]
Es liegt nur eine schwache Affinität zu cholinergen, insbesondere muskarinischen Neuronen vor, weswegen nur geringe anticholinerge bzw. kardiovaskuläre Nebenwirkungen auftreten. Die Wiederaufnahme von Noradrenalin oder Serotonin wird kaum beeinflusst und auch die Affinität zu β-adrenergen und dopaminergen Neuronen ist gering.[6] In einer Studie wurde, durch Opioid-Antagonisten-Gabe, die Wirkung von Mirtazapin auf opioide Rezeptoren bestätigt. Mirtazapin besitzt eine hohe Affinität zum κ3-Opioid-Rezeptor und in geringerem Maße zum μ-Opioid-Rezeptor.[7]
Die Rezeptor-Affinitäten betragen:
- 5-HT1A Rezeptor (Ki=18nM; IC50=1,000nM) [8]
- 5-HT2A Rezeptor (Ki = 69 nM)
- 5-HT2B Rezeptor (Ki = ? (~20x niedriger als für 5-HT2A/2C))[9]
- 5-HT2C Rezeptor (Ki = 39 nM)
- 5-HT3 Rezeptor (Ki = ? (ähnlich wie 5-HT2A/2C)[10]
- 5-HT7 Rezeptor (Ki = 265 nM)
- a1-Adrenozeptor (Ki = 608 nM (Ratte))
- a2A-Adrenozeptor (Ki = 20 nM)
- a2C-Adrenozeptor (Ki = 18 nM)
- H1 Rezeptor (Ki = 5.1 nM) [11]
- Muskarinischer Acetylcholinrezeptor (Ki = 794 nM (Ratte))
- D1 Rezeptor (Ki=4,167nM) [12]
- D2 Rezeptor (Ki=1,460nM) [11]
- D3 Rezeptor (Ki=5,723nM) [13]
- D4 Rezeptor (Ki=25nM) [11]
Mirtazapin hat auch Affinität zum Noradrenalin-Transporter und vielleicht auch zum Serotonin- und Dopamin-Transporter gezeigt (Ergebnisse des Tests nicht spezifiziert):
- Noradrenalin-Transporter (IC50=260nM) [14]
- Serotonin-Transporter (IC50=100nM) [15]
- Dopamin-Transporter (IC50=1,000nM) [16]
Die Wirkung von Mirtazapin wird vermutlich von seinen beiden Enantiomeren vermittelt, jedoch auf jeweils verschiedene Weise: Während das (S)-(+)-Enantiomer für die α2- und 5-HT2-Rezeptorblockade verantwortlich ist, bewirkt das (R)-(−)-Enantiomer die Blockade des 5-HT3-Rezeptors. [5]
Verstoffwechselung (Pharmakokinetik)
Mirtazapin wird nach oraler Gabe schnell resorbiert, aber teilweise vor Übertritt in den Körperkreislauf (präsystemisch) in der Darmwand und in der Leber verstoffwechselt (metabolisiert). Die höchsten Plasmakonzentrationen sind spätestens nach zwei Stunden erreicht; die Bioverfügbarkeit beträgt etwa 50 %. Die Metabolisierung, vor allem durch N-Demethylierung, N-Oxidation und 8-Hydroxylierung, erfolgt in erster Linie über die Cytochrom P450 Isoenzyme CYP2D6 und CYP3A4. Bei einmal täglicher Verabreichung wird innerhalb von vier bis sechs Tagen ein Fließgleichgewicht erreicht. Die Plasmahalbwertszeit beträgt bei Erwachsenen 20 bis 40 Stunden. Der Hauptmetabolit Demethyl-Mirtazapin hat nur eine geringe pharmakologische Aktivität. Die Bildung anderer aktiver Metaboliten ist mengenmäßig unbedeutend.
Die pharmakokinetischen Eigenschaften von Mirtazapin sind nicht identisch für beide Enantiomere des Mirtazapin. So hat das (R)-(–)-Enantiomer eine längere Plasmahalbwertszeit als das (S)-(+)-Enantiomer (ca. 18 vs. ca. 10 Stunden). Auch wirkt sich ein genetischer CYP2D6-Polymorphismus auf die beiden Enantiomere unterschiedlich aus. Während die Verstoffwechselung des (R)-(–)-Enantiomers davon unbeeinflusst bleibt, muss bei sogenannten schwachen Metabolisierern (engl. poor metabolizers) mit einer deutlich längeren Halbwertszeit für das (S)-(+)-Enantiomer gerechnet werden. [17]
Klinische Angaben
Anwendungsgebiete (Indikationen)
Mirtazapin ist in Deutschland und der Schweiz ausschließlich zur Behandlung von depressiven Erkrankungen zugelassen. Nach einer vorläufigen Nutzenbewertung des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) gibt es keine Belege für eine Überlegenheit Mirtazapins gegenüber anderen Antidepressiva.[18]
Es wird außerhalb der zugelassenen Anwendungsgebiete (Off-Label Use) außerdem zur Therapie der generalisierten Angststörung(GAD),[19] sozialen Phobie,[20] Panikstörung,[21] Winterdepression (SAD)[22] und Schlafstörungen[23] eingesetzt. Außerdem wird Mirtazapin off-Label in der adjuvanten Schmerztherapie verwendet, wobei die vorhandenen Studiendaten für die wesentlich besser geprüften Trizyklika wie Amitriptylin sprechen. Off-Label kann Mirtazapin ferner zur Behandlung der posttraumatischen Belastungsstörung genutzt werden. Bei schweren Fällen lindert es die Symptome möglicherweise stärker als SSRI.[24]
Darreichungsformen
Mirtazapin existiert als Handelspräparat in Form von Filmtabletten und Schmelztabletten, sowie als Lösung zum Einnehmen. Eine parenterale Anwendung ist mit Konzentrat zur Bereitung von Infusionslösung möglich.
Unerwünschte Wirkungen
Besonders zu Beginn der Behandlung, aber auch für die gesamte Zeit der Einnahme, kann es zu sehr starker Müdigkeit und Trägheit kommen, da Mirtazapin sedierend wirkt. Häufig ist eine Gewichtszunahme aufgrund von Appetitsteigerung und Ödemen zu beobachten. Auch ein Anstieg der Cholesterinwerte wird berichtet.[25][26] Bei Kindern und Jugendlichen können Aggressivität und insbesondere verstärkte Suizidalität auftreten; auch fehlen für sie Langzeitdaten zur Sicherheit. Bei einem plötzlichen Absetzen treten mitunter Symptome (leichte Unruhe, vorübergehende Schlafstörungen, leichtes Schwitzen) auf. Weiterhin können in seltenen Fällen Missempfindungen der Haut, Albträume und Halluzinationen, Verwirrtheit und Krampfanfälle auftreten, und das extrapyramidalmotorische System kann erheblich gestört werden. Es wird von Knochenmarkdepression bei der Behandlung mit Mirtazapin berichtet.
Wechselwirkungen
Mirtazapin kann die zentralnervös-dämpfende Wirkung von Alkohol, vielen Benzodiazepinen und anderen sedierenden Arzneimitteln verstärken. Carbamazepin und Phenytoin erhöhen die Mirtazapin-Clearance um das Zweifache, mit der Folge, dass die Mirtazapin-Plasmakonzentrationen um 45–60 % sinken. Die Mirtazapin-Dosis muss eventuell angepasst werden. [27][28]
Anwendung in der Schwangerschaft und Stillzeit
Ausreichende Daten zur Anwendung von Mirtazapin bei schwangeren Frauen liegen nicht vor, was in der Nutzen-Risiko-Abwägung zu berücksichtigen ist. Tierversuche haben Risiken für die Föten gezeigt. Obwohl im Tierexperiment nur vernachlässigbare Mengen Mirtazapin in die Muttermilch übergingen, sollte aufgrund fehlender Humanstudien auf die Verwendung von Mirtazapin während der Stillzeit verzichtet werden.[29]
Absetzproblematik
Obwohl Mirtazapin nicht abhängig macht, kann ein plötzliches Absetzen von Mirtazapin manchmal zu Absetzerscheinungen führen. Die meisten Absetzerscheinungen sind leicht und selbstlimitierend. Die Stärke dieses Absetzsyndroms hängt sowohl von der Dauer der vorangegangenen Behandlung als auch der Höhe der Tagesdosen ab. Um Absetzsymptome wie etwa Übelkeit, Kopfschmerzen, Angstzustände, Schlafstörungen und Unruhe abzumildern, wird Mirtazapin ausschleichend abgesetzt.
Chemie und Stereoisomerie
Mirtazapin besitzt ein Stereozentrum am benzylischen Kohlenstoffatom, folglich gibt es zwei Stereoisomere die (R)-Form und die dazu spiegelbildliche (S)-Form. Die Fertigarzneimittel enthalten alle das Racemat [1:1-Gemisch der (R)-Form und der (S)-Form)] ist.
Unterschiede in der Kosten-Nutzen-Relation
Einige Medikamente zur Behandlung von Depressionen haben im Verhältnis zu ihrem Nutzen deutlich höhere Preise als andere. So lautet der Befund der ersten Kosten-Nutzen-Bewertung des Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) für die Wirkstoffe Venlafaxin, Duloxetin, Bupropion und Mirtazapin.[30]
Handelsnamen
Monopräparate: Remergil (D), Remeron (CH), div. Generika
Weblinks
- Arzneimittel-Kompendium der Schweiz: Mirtazapin-Präparate
- Mirtazapin. In: Erowid. (englisch)
- Blog zum Medikament Mirtazapin: meinwegausderangst.de/mirtazapin
Einzelnachweise
- ↑ 1,0 1,1 1,2 Datenblatt MIRTAZAPINE CRS (PDF) beim EDQM
- ↑ 2,0 2,1 2,2 Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.3. Georg Thieme Verlag KG, Stuttgart 2009.
- ↑ Datenblatt Mirtazapine bei Sigma-Aldrich (PDF).
- ↑ 4,0 4,1 Gillman, PK. (2006): A systematic review of the serotonergic effects of mirtazapine in humans: implications for its dual action status. Hum Psychopharmacol. 21(2): 117–25; PMID 16342227.
- ↑ 5,0 5,1 Fachinformation Mirtazapin]
- ↑ 6,0 6,1 6,2 6,3 medizin-medien.info – Mirtazapin – Stellenwert in der Depressionsbehandlung (PDF 371 KB)
- ↑ Shaul Schreiber, Avi Bleich and Chaim G. Pick: Venlafaxine and mirtazapine - Different mechanisms of antidepressant action, common opioid-mediated antinociceptive effects—A possible opioid involvement in severe depression? In: Journal of Molecular Neuroscience. 18. Jahrgang, 2002, S. 143–149, doi:10.1385/JMN:18:1-2:143.
- ↑ Unspecified as to whether it was active or inactive in this assay neither was its actions towards 5-HT1A specified; PMID=14640559 (IC50) and PMID=12109911 (Ki)
- ↑ T De Boer: The pharmacologic profile of mirtazapine. In: The Journal of clinical psychiatry. 57 Suppl 4. Jahrgang, 1996, S. 19–25, PMID 8636062.
- ↑ Kooyman AR, Zwart R, Vanderheijden PM, Van Hooft JA, Vijverberg HP: Interaction between enantiomers of mianserin and ORG3770 at 5-HT3 Rezeptors in cultured mouse neuroblastoma cells. In: Neuropharmacology. 33. Jahrgang, Nr. 3-4, 1994, S. 501–7, doi:10.1016/0028-3908(94)90081-7, PMID 7984289.
- ↑ 11,0 11,1 11,2 HV. Wikström, MM. Mensonides-Harsema, TI. Cremers, EK. Moltzen, J. Arnt: Synthesis and pharmacological testing of 1,2,3,4,10,14b-hexahydro-6-methoxy-2-methyldibenzo[c,f]pyrazino[1,2-a]azepin and its enantiomers in comparison with the two antidepressants mianserin and mirtazapine. In: J Med Chem. 45. Jahrgang, Nr. 15, Juli 2002, S. 3280-5.
- ↑ Unknown whether this is agonist or antagonist activity see - PMID=15771415
- ↑ J. Fernández, JM. Alonso, JI. Andrés, JM. Cid, A. Díaz, L. Iturrino, P. Gil, A. Megens, VK. Sipido: Discovery of new tetracyclic tetrahydrofuran derivatives as potential broad-spectrum psychotropic agents. In: J Med Chem. 48. Jahrgang, Nr. 6, März 2005, S. 1709-12, doi:10.1021/jm049632c.
- ↑ NN. Bogolepov, TV. Vorob'eva, GS. Burd, NI. Pavlovskaia: [Changes in the mitochondria of human cerebral cortex nerve cells as the result of strokes]. In: Zh Nevropatol Psikhiatr Im S S Korsakova. 75. Jahrgang, Nr. 7, 1975, S. 980-6.
- ↑ As above, plus whether the mirtazapine was active or inactive in the assay was unspecified, PMID=12109911
- ↑ A. Orjales, R. Mosquera, A. Toledo, MC. Pumar, N. García, L. Cortizo, L. Labeaga, A. Innerárity: Syntheses and binding studies of new [(aryl)(aryloxy)methyl]piperidine derivatives and related compounds as potential antidepressant drugs with high affinity for serotonin (5-HT) and norepinephrine (NE) transporters. In: J Med Chem. 46. Jahrgang, Nr. 25, Dezember 2003, S. 5512-32, doi:10.1021/jm0309349.
- ↑ Timmer, CJ. et al. (2000): Clinical pharmacokinetics of mirtazapine. Clin Pharmacokinet. 38(6): 461–474; PMID 10885584.
- ↑ IQWiG Vorbericht A05-20C Bupropion, Mirtazapin und Reboxetin bei der Behandlung der Depression.
- ↑ Gambi F, De Berardis D, Campanella D, et al.: Mirtazapine treatment of generalized anxiety disorder: a fixed dose, open label study. In: Journal of Psychopharmacology (Oxford, England). 19. Jahrgang, Nr. 5, September 2005, S. 483–487, doi:10.1177/0269881105056527, PMID 16166185.
- Goodnick PJ, Puig A, DeVane CL, Freund BV: Mirtazapine in major depression with comorbid generalized anxiety disorder. In: The Journal of Clinical Psychiatry. 60. Jahrgang, Nr. 7, Juli 1999, S. 446–448, PMID 10453798.
- ↑ Van Veen JF, Van Vliet IM, Westenberg HG: Mirtazapine in social anxiety disorder: a pilot study. In: International Clinical Psychopharmacology. 17. Jahrgang, Nr. 6, November 2002, S. 315–317, doi:10.1097/00004850-200211000-00008, PMID 12409686 (wkhealth.com).
- Muehlbacher M, Nickel MK, Nickel C, et al.: Mirtazapine treatment of social phobia in women: a randomized, double-blind, placebo-controlled study. In: Journal of Clinical Psychopharmacology. 25. Jahrgang, Nr. 6, Dezember 2005, S. 580–583, PMID 16282842 (wkhealth.com).
- Mörtberg E: Mirtazapine reduces social anxiety and improves quality of life in women with social phobia. In: Evidence-based Mental Health. 9. Jahrgang, Nr. 3, August 2006, S. 75, doi:10.1136/ebmh.9.3.75, PMID 16868194 (bmj.com).
- Mrakotsky C, Masek B, Biederman J, et al.: Prospective open-label pilot trial of mirtazapine in children and adolescents with social phobia. In: Journal of Anxiety Disorders. 22. Jahrgang, Nr. 1, 2008, S. 88–97, doi:10.1016/j.janxdis.2007.01.005, PMID 17419001.
- Liappas J, Paparrigopoulos T, Tzavellas E, Christodoulou G: Alcohol detoxification and social anxiety symptoms: a preliminary study of the impact of mirtazapine administration. In: Journal of Affective Disorders. 76. Jahrgang, Nr. 1–3, September 2003, S. 279–284, doi:10.1016/S0165-0327(02)00094-0, PMID 12943960 (elsevier.com).
- ↑ Sarchiapone M, Amore M, De Risio S, et al.: Mirtazapine in the treatment of panic disorder: an open-label trial. In: International Clinical Psychopharmacology. 18. Jahrgang, Nr. 1, Januar 2003, S. 35–38, doi:10.1097/01.yic.0000047780.24295.3e, PMID 12490773.
- Boshuisen ML, Slaap BR, Vester-Blokland ED, den Boer JA: The effect of mirtazapine in panic disorder: an open label pilot study with a single-blind placebo run-in period. In: International Clinical Psychopharmacology. 16. Jahrgang, Nr. 6, November 2001, S. 363–368, doi:10.1097/00004850-200111000-00008, PMID 11712626 (wkhealth.com).
- Carpenter LL, Leon Z, Yasmin S, Price LH: Clinical experience with mirtazapine in the treatment of panic disorder. In: Annals of Clinical Psychiatry : Official Journal of the American Academy of Clinical Psychiatrists. 11. Jahrgang, Nr. 2, Juni 1999, S. 81–86, PMID 10440525.
- Carli V, Sarchiapone M, Camardese G, Romano L, DeRisio S: Mirtazapine in the treatment of panic disorder. In: Archives of General Psychiatry. 59. Jahrgang, Nr. 7, Juli 2002, S. 661–662, doi:10.1001/archpsyc.59.7.661, PMID 12090820 (ama-assn.org).
- Ribeiro L, Busnello JV, Kauer-Sant'Anna M, et al.: Mirtazapine versus fluoxetine in the treatment of panic disorder. In: Brazilian Journal of Medical and Biological Research = Revista Brasileira De Pesquisas Médicas E Biológicas / Sociedade Brasileira De Biofísica ... [Et Al.] 34. Jahrgang, Nr. 10, Oktober 2001, S. 1303–1307, PMID 11593305 (scielo.br).
- ↑ Mirtazapine in seasonal affective disorder (SAD): a preliminary report. Abgerufen am 13. Januar 2011.
- ↑ Winokur A, DeMartinis NA, McNally DP, Gary EM, Cormier JL, Gary KA: Comparative effects of mirtazapine and fluoxetine on sleep physiology measures in patients with major depression and insomnia. In: The Journal of Clinical Psychiatry. 64. Jahrgang, Nr. 10, Oktober 2003, S. 1224–1229, PMID 14658972 (psychiatrist.com).
- Kim SW, Shin IS, Kim JM, et al.: Effectiveness of mirtazapine for nausea and insomnia in cancer patients with depression. In: Psychiatry and Clinical Neurosciences. 62. Jahrgang, Nr. 1, Februar 2008, S. 75–83, doi:10.1111/j.1440-1819.2007.01778.x, PMID 18289144.
- Cankurtaran ES, Ozalp E, Soygur H, Akbiyik DI, Turhan L, Alkis N: Mirtazapine improves sleep and lowers anxiety and depression in cancer patients: superiority over imipramine. In: Supportive Care in Cancer : Official Journal of the Multinational Association of Supportive Care in Cancer. 16. Jahrgang, Nr. 11, November 2008, S. 1291–1298, doi:10.1007/s00520-008-0425-1, PMID 18299900.
- ↑ Korean J Psychopharmacol., Dezember 2002 ;13(4): S. 254–261. Korean.
- Chung, MY. et al. (2004): Efficacy and tolerability of mirtazapine and sertraline in Korean veterans with posttraumatic stress disorder: a randomized open label trial. Hum. Psychopharmacol. 19(7), S. 489–494; PMID 15378676.
- Zohar, J. et al. (2002): Double-blind placebo-controlled pilot study of sertraline in military veterans with posttraumatic stress disorder. J. Clin. Psychopharmacol. 22(2): 190–195; PMID 11910265.
- Davidson JR, Weisler RH, Butterfield MI, et al.: Mirtazapine vs. placebo in posttraumatic stress disorder: a pilot trial. In: Biological Psychiatry. 53. Jahrgang, Nr. 2, Januar 2003, S. 188–191, doi:10.1016/S0006-3223(02)01411-7, PMID 12547477 (elsevier.com).
- Kim W, Pae CU, Chae JH, Jun TY, Bahk WM: The effectiveness of mirtazapine in the treatment of post-traumatic stress disorder: a 24-week continuation therapy. In: Psychiatry and Clinical Neurosciences. 59. Jahrgang, Nr. 6, Dezember 2005, S. 743–747, doi:10.1111/j.1440-1819.2005.01447.x, PMID 16401254.
- Bahk WM, Pae CU, Tsoh J, et al.: Effects of mirtazapine in patients with post-traumatic stress disorder in Korea: a pilot study. In: Human Psychopharmacology. 17. Jahrgang, Nr. 7, Oktober 2002, S. 341–344, doi:10.1002/hup.426, PMID 12415552.
- Chung MY, Min KH, Jun YJ, Kim SS, Kim WC, Jun EM: Efficacy and tolerability of mirtazapine and sertraline in Korean veterans with posttraumatic stress disorder: a randomized open label trial. In: Human Psychopharmacology. 19. Jahrgang, Nr. 7, Oktober 2004, S. 489–494, doi:10.1002/hup.615, PMID 15378676.
- Alderman CP, Condon JT, Gilbert AL: An Open-Label Study of Mirtazapine as Treatment for Combat-Related PTSD(July/August). In: The Annals of Pharmacotherapy. 43. Jahrgang, Nr. 7, Juli 2009, S. 1220–1226, doi:10.1345/aph.1M009, PMID 19584388.
- Lewis JD: Mirtazapine for PTSD nightmares. In: The American Journal of Psychiatry. 159. Jahrgang, Nr. 11, November 2002, S. 1948–1949, doi:10.1176/appi.ajp.159.11.1948-a, PMID 12411239 (psychiatryonline.org)..
- ↑ Mitchell D. Feldman & John F. Christensen (Hrsg.): Behavioral Medicine: A Guide for Clinical Practice: A Practical Guide. Mcgraw Hill Medical; 3. Auflage, 2007, S. 219.
- ↑ Alan F. Schatzberg, u.a. (Hrsg.): Manual of Clinical Psychopharmacology. 6. Auflage, Amer Psychiatric Pub Inc 2007, S. 94.
- ↑ Fachinformation des Arzneimittel-Kompendium der Schweiz: Remeron®; Stand der Informationen: Dezember 2007.
- ↑ Gebrauchsinformation: mirtazapin-biomo 15 mg Filmtabletten; Stand: 02/2008.
- ↑ Schweizer Fachinformation Remeron; Stand: August 2006.
- ↑ Kosten-Nutzen-Bewertung von Venlafaxin, Duloxetin, Bupropion und Mirtazapin im Vergleich zu weiteren verordnungsfähigen medikamentösen Behandlungen Übersicht zum Verfahren des IQWiG